Em outubro de 2024, a Agência Nacional de Vigilância Sanitária (Anvisa) clarificou questões acerca do uso de autotestes em farmácias. Esta regulamentação foi destacada na segunda edição do Perguntas e Respostas referente à RDC nº 786/2023. Segundo Fernanda Alcântara, farmacêutica e especialista na área, os autotestes não podem ser usados em serviços farmacêuticos presenciais. A decisão visa a garantir a segurança dos consumidores.
Segundo informações da Ascoferj, os autotestes, como os de glicemia, gravidez, HIV e intolerância ao glúten, continuam disponíveis para compra em farmácias, mas seu uso deve ocorrer em domicílio. A prática tem o objetivo de evitar possíveis riscos associados ao uso inadequado desses dispositivos em ambientes farmacêuticos, que não seriam adequados para tal fim.
Como os Autotestes Foram Impactados em Serviços Farmacêuticos?
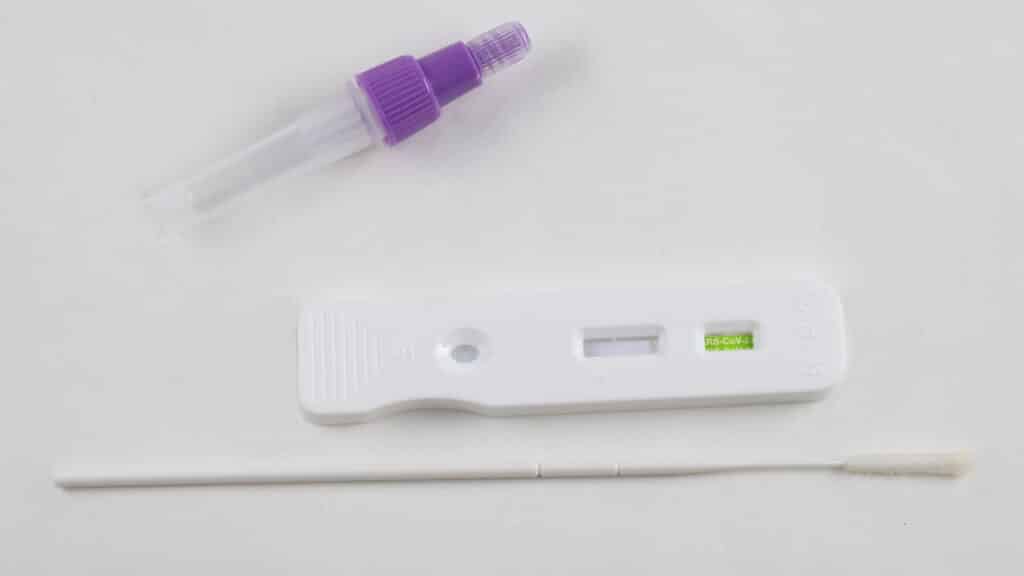
A Anvisa determinou que os autotestes não são adequados para uso em ambientes farmacêuticos devido a possíveis riscos ao consumidor. A agência considera que, sem a supervisão adequada ou ambientes controlados, os resultados desses testes podem ser interpretados de forma incorreta. No entanto, os farmacêuticos ainda podem prestar assistência educacional sobre o uso dos autotestes antes que os clientes os utilizem em casa.
Dentro das salas de serviços farmacêuticos, é permitida a utilização de equipamentos profissionais que sejam homologados pela Anvisa. Essa restrição visa assegurar que os procedimentos realizados sigam padrões de precisão e segurança. A Clinicarx, uma empresa de tecnologia em saúde, oferece informação sobre fornecedores que disponibilizam esses equipamentos para as farmácias.
O que o Futuro Reserva para os Testes em Farmácias em 2025?
Para 2025, espera-se a introdução de novos testes rápidos no mercado. Segundo Fernanda Alcântara, testes como hemograma e leucograma podem ser autorizados para uso em ambientes farmacêuticos. A autorização desses testes proporcionará melhores condições para os farmacêuticos correlacionarem dados clínicos, auxiliando no cuidado ao paciente e na colaboração com outros profissionais de saúde, como médicos.
Quais as Normas em Vigor para o Uso de Equipamentos de Diagnóstico?
Além da RDC nº 786/2023, há outras regulamentações que impactam o funcionamento das farmácias, como a RDC nº 44/2009. Esta última envolve boas práticas farmacêuticas e está em revisão com previsão para mudanças no primeiro semestre de 2025. Ambas as regulamentações estabelecem diretrizes complementares para a prestação de serviços farmacêuticos, destacando a necessidade de documentar e entregar ao paciente os laudos dos exames realizados na farmácia.
Principais Normas e Regulamentações
- ANVISA (Agência Nacional de Vigilância Sanitária): No Brasil, a ANVISA é o órgão responsável por regular os produtos médicos, incluindo os equipamentos de diagnóstico. As normas da ANVISA estabelecem requisitos para a fabricação, importação, distribuição e uso desses equipamentos, visando garantir a segurança e a eficácia dos procedimentos diagnósticos.
- FDA (Food and Drug Administration): Nos Estados Unidos, a FDA é a agência reguladora responsável pela segurança dos alimentos, medicamentos e produtos médicos, incluindo os equipamentos de diagnóstico. As normas da FDA estabelecem requisitos rigorosos para a aprovação e o uso desses equipamentos.
- IEC (International Electrotechnical Commission): A IEC é uma organização internacional que desenvolve normas técnicas para equipamentos elétricos e eletrônicos, incluindo os equipamentos médicos. As normas da IEC fornecem requisitos de segurança e desempenho para esses equipamentos.


