A Anvisa aprovou, em 30 de março de 2026, o registro do Enflonsia® (clesrovimabe), fabricado pela Merck Sharp & Dohme. O medicamento é uma solução injetável indicada para prevenir infecções graves causadas pelo vírus sincicial respiratório em recém-nascidos e lactentes.
Como o novo medicamento aprovado pela Anvisa atua nos bebês?
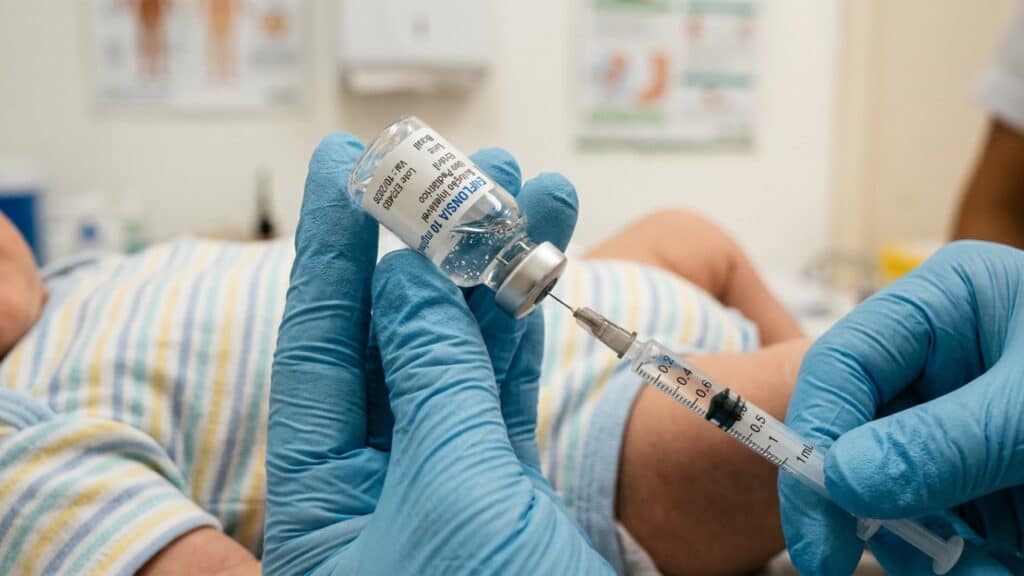
O produto funciona como um anticorpo monoclonal que oferece proteção direta durante os períodos de maior circulação do vírus. A administração é intramuscular e foca especialmente em crianças nos primeiros meses de vida, fase em que a bronquiolite costuma ser mais severa.
Bebês prematuros ou com cardiopatias congênitas possuem prioridade, pois apresentam maior risco de complicações respiratórias. Segundo a Agência Nacional de Vigilância Sanitária, pacientes submetidos a cirurgias cardíacas complexas podem necessitar de doses adicionais para manter os níveis de proteção adequados.
Qual é o impacto do VSR na saúde pública brasileira?
O vírus sincicial respiratório é o principal agente causador de infecções no trato respiratório inferior em crianças menores de dois anos. Dados do Ministério da Saúde indicam que ele responde por cerca de 80% dos casos de bronquiolite e até 60% dos quadros de pneumonia em crianças nessa faixa etária.
A gravidade da situação é evidenciada pelo alto número de hospitalizações no primeiro ano de vida. Confira as estatísticas de impacto do vírus no Brasil:
- Uma em cada cinco crianças infectadas necessita de atendimento ambulatorial.
- Uma em cada 50 crianças é hospitalizada ao longo do primeiro ano de vida.
- Em 2025, foram registradas 42.450 infecções, das quais 34.988 em menores de dois anos.
- Cerca de 20 mil bebês menores de um ano são internados anualmente no país.
A aprovação feita pela Anvisa reforça o arsenal terapêutico para reduzir a sobrecarga nos leitos de UTI pediátrica. A medida é um passo estratégico para diminuir a mortalidade infantil associada a doenças respiratórias sazonais.
Como funciona a campanha de vacinação do SUS contra o vírus?
A partir de dezembro de 2025, o governo federal iniciou a imunização de gestantes a partir da 28ª semana de gravidez, com a incorporação da vacina ao Calendário Nacional de Vacinação. Essa estratégia permite a transferência de anticorpos da mãe para o bebê, garantindo uma proteção inicial crucial logo após o nascimento pelo Sistema Único de Saúde — estudos clínicos indicam eficácia de 81,8% na prevenção de quadros graves nos primeiros 90 dias de vida.
O novo medicamento complementa essa rede de proteção, agindo diretamente no organismo do recém-nascido que não recebeu imunidade materna suficiente. De acordo com o Ministério da Saúde, o foco é cercar o vírus em diversas frentes para garantir um desenvolvimento saudável nos primeiros anos.
Onde consultar a resolução oficial da aprovação?
A decisão técnica foi formalizada por meio da Resolução (RE) 1.214/2026, disponível para consulta pública. O documento detalha as exigências de armazenamento, transporte e os critérios rigorosos de segurança que a farmacêutica deve seguir para comercializar o produto no país.
A transparência desses dados permite que médicos e gestores hospitalares planejem a introdução da terapia nos protocolos de atendimento. O acesso à informação oficial no Diário Oficial da União garante que a sociedade acompanhe as etapas de validação de novas tecnologias em saúde.
Quais são as orientações para pais e responsáveis?
A recomendação é que as famílias mantenham o acompanhamento pediátrico em dia e fiquem atentas aos primeiros sinais de esforço respiratório ou febre. O uso do Enflonsia® deve ser sempre orientado por um profissional de saúde, respeitando o calendário de circulação viral da região.
Prevenir o contato com pessoas gripadas e manter a higienização das mãos são medidas simples que potencializam o efeito do medicamento. Com a chegada de novas opções terapêuticas aprovadas pela Anvisa em 2026, a expectativa é de um cenário muito mais controlado e seguro para as crianças brasileiras.


